--- NKT細胞癌免疫治療 ---
はじめに
当院の院長は、腫瘍外科医(surgical oncologist)として30年以上癌治療を行ってきた癌治療認定医機構癌治療認定医で、日本外科学会、消化器外科学会、癌治療学会にも所属し、専門医として診療してきました。特に困難な食道癌手術における第一人者でもあります。
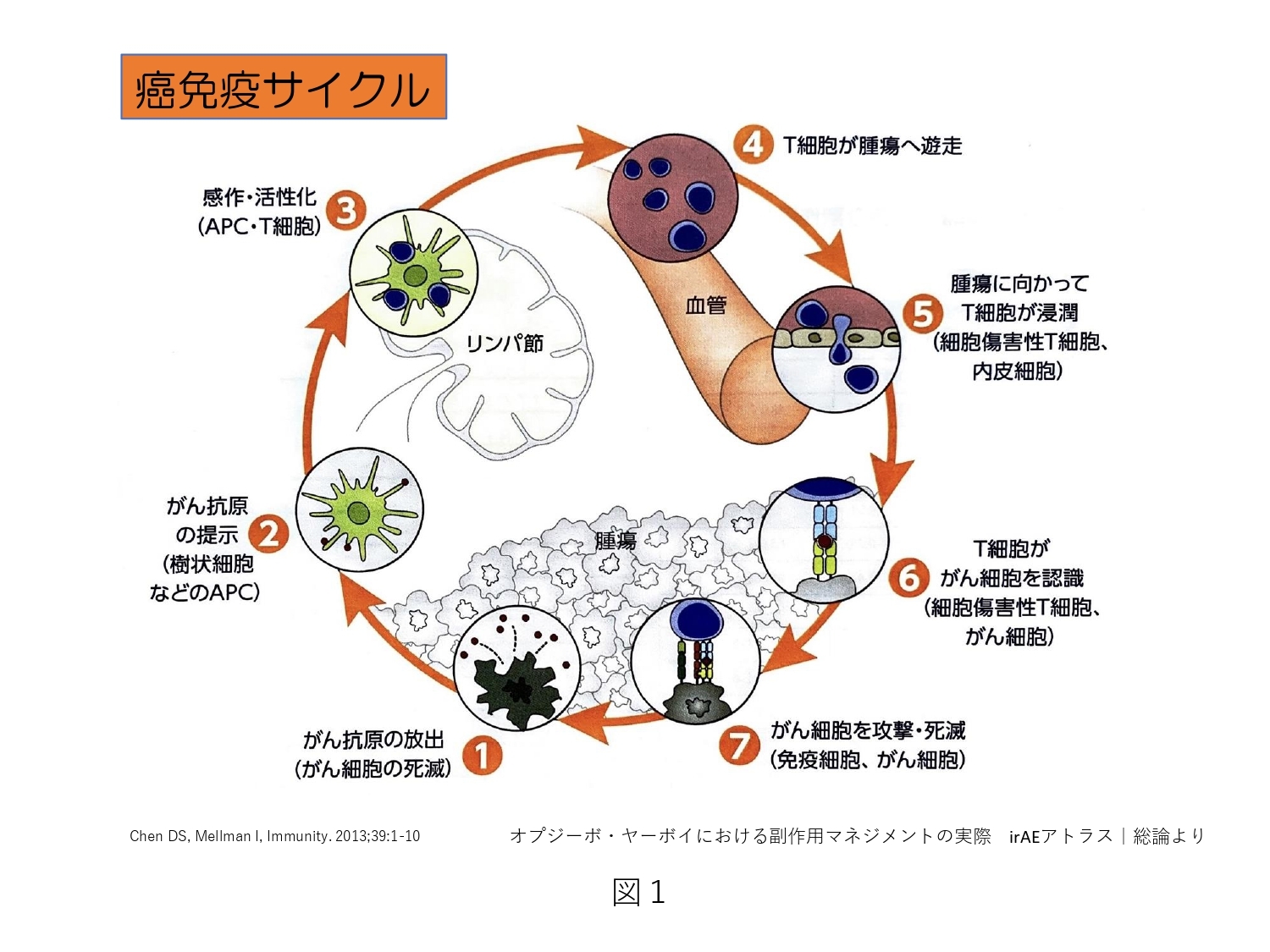
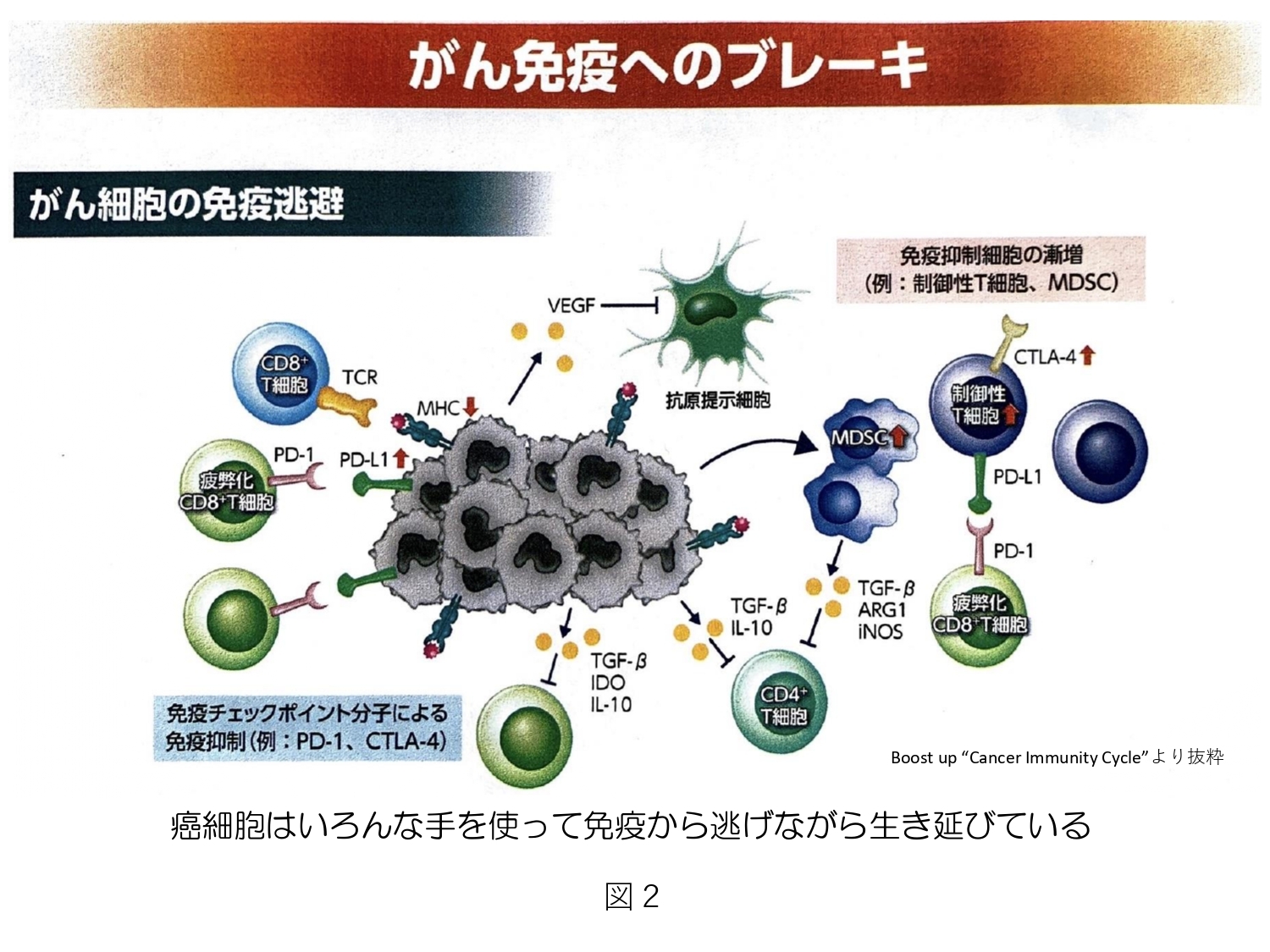
癌を根絶する方法は、癌組織を細胞レベルで取り除くことですので、癌組織を被膜に包んだままの状態で愛護的に切除しなければなりません。従って、癌が手術可能な範囲に限局していなければなりませんし、外科医の技術によっても根治度に差が生まれます。放射線治療も進化していますが、照射する部位のみの局所の治療です。癌病巣が転移や浸潤などで広がっている場合は全身治療となり、化学療法(抗癌剤治療)が選択されます。分子標的薬など新薬の開発があとを絶ちませんが、確実に癌を治すガイドラインは存在しません。しかし、化学療法を画期的に進化させたオプジーボ(ニボルマブ)は、まさしく7step癌免疫サイクル(図1)に示す免疫発動機序を利用したものです。癌細胞から発現する癌抗原を樹状細胞が認識し、抗原提示細胞(APC)としてT細胞やNKT細胞に癌抗原を提示・認識させ攻撃を指示します。癌細胞は免疫細胞攻撃部隊のターゲットにならないように巧みに逃れていて(図2)、これを免疫学的寛容(癌細胞の免疫逃避)と呼びますが、オプジーボは、免疫を逃れるために癌細胞が作り上げた隠れ蓑を剥がし、これにより免疫細胞が攻撃目標を捉えることができ、癌免疫サイクルが回り始めるという理論です。
院長は外科医として、手術で癌を切除してきましたが、この免疫細胞も細胞レベルで癌細胞を手術する名外科医であると考えています。
米国メモリアル・スローン・ケタリングがんセンターの腫瘍内科クリストファー・クレバノフ医師は、T細胞やNKT細胞などの免疫細胞は生物学的に最も驚くべきトリックを行うと言います。この免疫細胞には、癌細胞の表面にある抗原タンパクを認識し結合する受容体があり、それらが鍵と鍵穴のように結合すると、免疫細胞が食指を伸ばし、癌細胞に穴をあけて破壊します。まさに免疫細胞が癌細胞に取りつき、穴をあけようとする瞬間の写真(写真1)が、Yahoo!ニュースで紹介されました。
米国マウントサイナイ・アイカーン医科大学の血液内科・腫瘍内科の専門家ニーナ・バルドワジ氏は、この治療はまだ臨床研究段階にあり、残念ながら大きな腫瘍の完全除去に必要な数のNKT細胞を生み出すのは難しいと話しています。
しかし私たちは、各治療単独ではなく、手術や放射線治療、各種抗癌剤そして免疫治療を組み合わせた「集学的治療」を行うことが根治に結びつくと考えています。フランスのDr. J.Y. Blayらが、免疫チェックポイント阻害剤の投与を術前に行うことで、癌肉腫患者の再発率を低下させたと報告しました。このことからも免疫治療は手術成績に貢献すると判断され、これらの集学的治療が癌治療を大きく前進させると推測されます。
FOLFOX※1やXELOX※2のような各種抗癌剤を組み合わせて行う化学療法のように、抗癌剤で癌組織を攻撃する間に、免疫治療を併用することで、後に述べる癌幹細胞も叩き、再発/再増殖を防ぐ効果が期待できます。陽子線・重粒子線との併用が効果的であったという報告もあります。また腫瘍栄養血管動注療法や腹腔内投与などの選択肢やBNCT(ホウ素中性子補捉療法)、光免疫治療との連携など、癌治療の新たな分野が考案されてきています。癌の集学的治療は、保険診療の枠を超えて研究・開発され、広がりつつあります。
※1レジメン:フルオロウラシル+レボホリナート+オキサリプラチン
※2レジメン:ゼローダ+オキサリプラチン
最近では、千葉大学で頭頸部癌に対するiPS-NKT細胞治療の治験が行われています。これは健常者から採取した血液でiPS細胞を作成し、これをNKT細胞に分化誘導したもの(iPS-NKT細胞)を患者の腫瘍栄養血管から動注するものです(下図)。
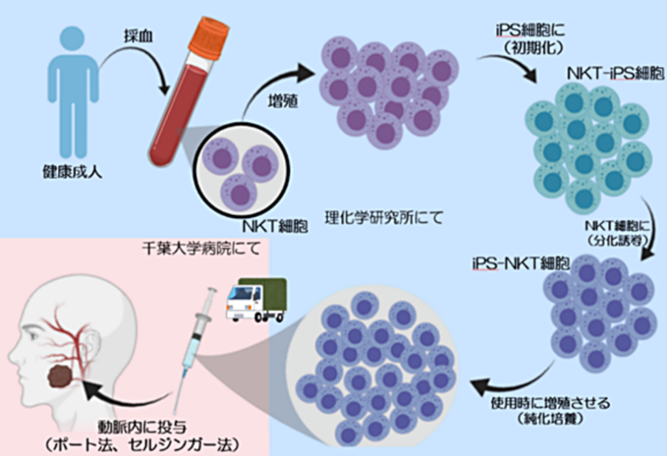
▶国立研究關発法人目本医療研究開発機構(2020年6月プレスリリース)
癌の3大治療法は、手術・放射線治療・化学療法です。前述した通り、手術と放射線治療は局所治療ですので、治療範囲を超えて広がっている癌は、全身治療である化学療法を選択することになります。抗癌剤によって癌細胞は傷害され死滅して行きますが、ここで注意しなければならないことは、癌組織の幹細胞、すなわち癌幹細胞には抗癌剤が効かないということです。私たちの体は組織を新鮮に保つために、細胞が絶えず入れ替わり続けるため、再生して補充する能力を持った幹細胞(stem cell)という細胞が備わっています。iPS細胞も幹細胞の一つですが、癌組織にもこの幹細胞が存在し、癌の形成・成長に重要な役割を果たすだけでなく、転移・再発にも深く関与すると考えられています。癌幹細胞は、普段は静止期にあり、活動期の癌細胞にしか作用できない抗癌剤は効きません。一度縮小しても再発するのはこの幹細胞が原因ではないかと考えられています。免疫細胞は癌幹細胞も攻撃しますので、理論的には癌組織を完全に排除できます。
こういった癌免疫治療の研究・開発によって、将来免疫治療が癌治療の根幹となる可能性も実証され始めています。ここで、癌幹細胞についての説明を記載します。
幹細胞は、体組織の幹となる細胞で生命維持に不可欠です。しかし癌幹細胞は、 (1)自分のコピーをつくる、(2)分化する、 (3)薬剤を細胞の外へ汲み出す、(4)通常は静止期で、増殖期に作用する抗癌剤が効きにくい、など幹細胞がもつ機能を駆使して抗癌剤耐性を示しながら、様々な顔つきの“子分”癌細胞へと分化し、癌を不均一な細胞集団(組織)へと成長させます。癌の大半を占める分化した癌細胞が抗癌剤により消滅する中、治療後も生き残るごく一部の癌幹細胞がその後の転移・再発に深く関与すると考えられるため、癌根治を目指した治療法を開発する上で、癌幹細胞は重要な標的の1つとなっています。
(Yakult中央研究所健康用語の基礎知識より引用 https://institute.yakult.co.jp/dictionary/word_3910.php )
当院が行う癌免疫治療の紹介をしますが、その前に、癌はDNAが壊れた細胞の病気ですので、癌を理解して頂くために、(1)で基本的な「細胞の話」をします。
必要のない方は『(2)NKT細胞による癌免疫治療の実際』からお読みください。
(1)細胞の話
細胞核の中のDNAには生体が生きるために必要な遺伝子情報プログラムが暗号化されて詰め込まれています。その暗号は、細胞間での通信に使う言語や、怪我や病気になったときの緊急事態に対する救済処置マニュアルなど、多数のプログラムが存在します。
例えば、指を刃物で1cm程度切ったとします。もちろん命に関わる傷ではありませんが、受傷した局所ではてんやわんやの大騒ぎになっています。毛細血管が切断され下流の孤立した組織は酸素不足に陥るため、HIF-1(低酸素誘導性転写因子)というシグナルを発信して周囲に助けを求めます。このシグナルが発信されると組織は自動的に省エネモードに切替り、周囲組織からは酸素供給支援が始まります。出血に対しては止血のシグナルが周囲に送られ、血小板が集積して血栓を作り、切断面の血管からの出血を止めます。その後、血流を再開させるために血栓を溶かし、組織が壊死に陥らないよう新しく血管を作り始めます(血管新生)。そして酸素や栄養を孤立した組織に供給した上で、負傷部位の修復が始まり治癒に向かうのです。これが創傷治癒過程初期の仕組みですが、DNAがタンパク質をシグナルにした言語を使って会話をし、人命救護ならぬ細胞救助を行っています。体内ではそういった完璧なライフラインが存在しています。私たちの住むエリアのインフラより素晴らしいシステムが体内には備わっています。ただ癌細胞も、この素晴らしい仕組みを悪用していることが分かっています。
細胞は生きるために細胞分裂し、DNAもコピーされます。コピーするたびにDNAの両端にあるテロメアというコピー読み取りに重要な部分が消費されて短くなって行き、最後はコピーができなくなります。これが老化であり細胞死(apotosis)です。細胞は生きるという意志と共に死ぬという意志を持っていることになります。細胞の意志というよりDNAの意思です。老化して死ぬ細胞がいなければ、細胞分裂して増えた細胞は腫瘍組織になってしまいます。秩序を保って大きさや形状が変化しないよう、細胞のDNAが組織をコントロールしています。
ところが、癌細胞は生きるというDNAの意志が強く、死ぬ(apotosis)という選択をしなくなった細胞です。細胞分裂し、増殖し続けた結果、腫瘤(腫瘍)になるのです。老化しても生き続けるので、途中壊死に陥る細胞も出現し、壊死した組織は臭気を放つようになります(癌性悪液質)。腫瘍が増殖すると、その中心部は酸素や栄養が行かず、組織が悲鳴を上げ、周囲組織に救援を求めてHIF-1シグナルを出し、血管新生を起こし、さらに苦しくなると保身のために転移という手段を選択します。まず DNAを検索し「間質細胞への変異」というジャンルを開き、白血球のような間質細胞に変化し、アメーバのように歩き始めます。歩いて遊走し、リンパ液や血液を泳いで、別組織にたどり着くと、今度はDNAからその組織のIDを手に入れ、その住民になりすまして転移を完成させます。IDがあれば、見回りの免疫細胞が組織の異物である癌細胞を、敵だと見抜くことができないため、排除できません(免疫学的寛容)。そして間質系線維細胞を呼び寄せ砦を築いて行くのです。
生物が地球上に誕生した40億年前から大災害や微生物感染、放射線などの危機を経験しながらDNAは少しずつ成長・発達・変異を遂げ、生存し続けた結果、どの様な事態にも対応できるマニュアルを作り上げました。癌細胞も外界からの攻撃をしのぐマニュアルを使用し、治療という攻撃から身を守ることができます。さらに癌細胞はDNA中の蛋白シグナルを使い、周囲の細胞たちと会話しながら生きています。40億年かけてDNAに詰め込んだ情報を使って、生きるための努力をしているわけです。酸素や栄養が足りないときには、オレオレ詐欺のように、他の細胞をだまして奪い取ることができます。
癌免疫担当細胞の説明
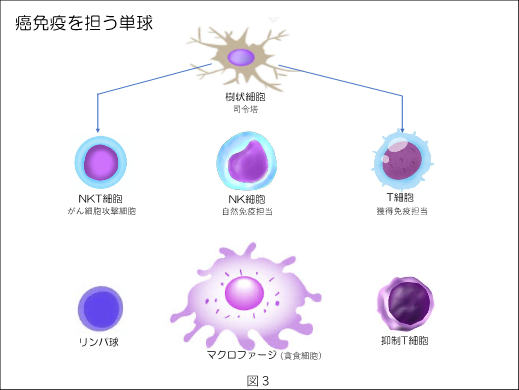
私たちが持つ免疫は、主に白血球が担います。白血球は顆粒球、リンパ球そして単球に分類されます。リンパ球も単球の一種ではありますが、癌免疫の中枢を担うのは単球(図3)です。単球(monocyte)は単核球とも呼ばれ、数種類に分類されます。その中で癌に対して攻撃を担う細胞として、注目されるのがNK細胞とT細胞、そしてその両方の機能と性質を併せ持つNKT細胞です。理研免疫の谷口らが、特にNKT細胞が癌細胞に対して強い攻撃力を持つことを確認しました。しかしヒトの血液中にわずかしか存在しません(0.01%)。そしてNKT細胞とT細胞に癌攻撃の指示を与える単球が樹状細胞(dendritic cell)です。
様々な単球が、自然免疫と獲得免疫に分かれ活躍しています。外敵と判断した異物に対して即座に対応するNK細胞は、非常に強い攻撃力を持っているのですが、指示に従って癌細胞を攻撃することはできません。T細胞は攻撃対象であることを樹状細胞(抗原提示細胞)から指示されて攻撃を開始しますが、NK細胞ほどの攻撃力がないのが欠点です。その両方の長所を持つNKT細胞を利用するのが最も効果的な癌免疫治療であるとされ、NKT細胞による癌免疫治療が開発されてきました。癌治療は攻撃目標が癌細胞ですので、目的通りに免疫細胞が動くことが必要です。樹状細胞の指令を受けてNKT細胞が癌細胞に取りつき破壊する仕組みが、理研免疫が着目し研究してきた方法です。
(2)NKT細胞による癌免疫治療の実際(癌免疫トライアングル)
(α-Galactosyl Ceramide刺激自己樹状細胞を用いたNKT細胞標的治療)
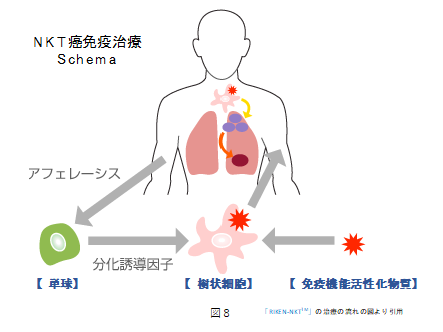
癌免疫治療として免疫担当細胞を活用する様々な方法が試されてきました。しかし前述したように、最も効果的な方法としてNKT細胞が注目され、この細胞を直接採取して培養増殖させ、身体に再投与する方法が試されました。後述する成分採血(apheresis)という方法で単球を採取し、単球をサイトカインであるインターロイキン(Interleukin:IL-2,-7,-12)によってNKT細胞に分化誘導し、数億個まで培養し、凍結した状態で保存し、解凍したものを週2回ずつ投与する方法が主流でしたが、NKT細胞が短命であることやインターロイキンが混入することで発熱するため、治療効果が低い上に苦痛も伴うことが分かりました。また、これらすべての細胞に役割を与えないまま、むやみに何種類もの免疫細胞を混入して投与しても、癌細胞を攻撃する仕組みが成り立たないことも疑問が持たれます。
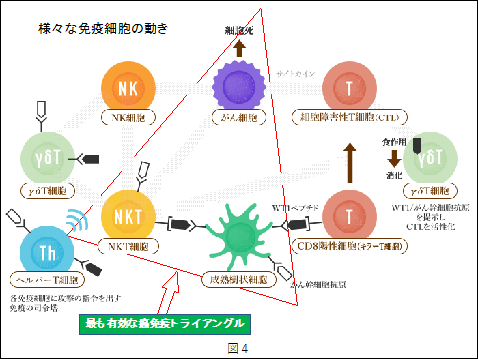
そこでNKT細胞を効果的に活用するために、理研免疫再生医学研究所が注目し開発した方法を図4に示します。重要なのは癌免疫トライアングルで、癌抗原と同等のシグナルを持つα- Galactosyl Ceramide(αGalCel)を認識した樹状細胞が、その情報をNKT細胞に伝え、癌細胞を攻撃させ、死滅させる治療です。全血中3〜9%の単球(約10億個)を採取し、それを樹状細胞に分化させます。この細胞に癌抗原と同じ効力を持つαGalCelを接着させて成熟樹状細胞(約1億個)とし、これを体内に戻し、体内のNKT細胞に対して、長期的に癌細胞への攻撃命令を出します。NKT細胞は1種類の抗原受容体しか持たず、この場合、癌抗原を持つ癌細胞を攻撃し続けます。従って、効率的に癌免疫治療が得られる理想的な免疫治療なのです。
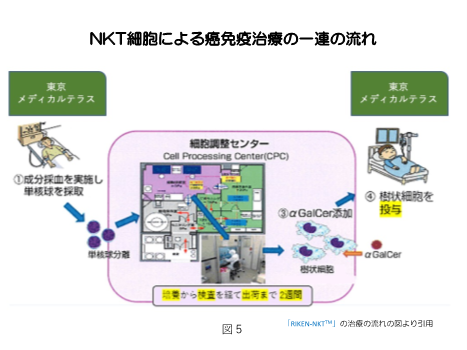
①単球の採取(アフェレーシス=血液成分分離採取)
この過程は当クリニック内で行います(図5左側:東京メディカルテラスの部分)。
〈手技説明〉
患者さんを仰臥位とし、局麻下に鼠径部の大腿静脈に12Frのtriple lumen catheterをcanulationし、約1〜2時間血液を体外循環させ、遠心分離型血液成分分離装置(COM.TEC)にて末梢血単核球(PBMC)を2x109個程度採取します。血液量としては、PBMCを主成分とした血液を150mL程度と血漿50mLを採取することになります。体外循環総血液量は4500mLを目安とし、医師が脱血を用の静脈を確保できないと判断した場合には、動脈から実施することもあります。
②採取後採取した単球成分は、4時間程度4℃前後の冷蔵保存とし、細胞調整センター(京大桂VP・CPC 施設番号FA5190003)に、専門運搬業者によって移送します。
図5中央:細胞調整センターの部分です。
③細胞調整センターでは、採取した単球に分化誘導因子(インターロイキン4)を添加して樹状細胞に分化させ(図6)、約1週間で平均8X107個の樹状細胞を培養しています。
培養開始6日目に樹状細胞に類癌細胞抗原(α-Galactocylceramide)を接着させて成熟させます。これによりNKT細胞やγσT細胞に標的(target)の指示を与える細胞である抗原提示細胞(APC)となり、癌細胞への攻撃準備が完成します。
この成熟した樹状細胞を血漿に入れ、-70℃に凍結したものを数個作成します。
④−70℃に凍結したまま、樹状細胞溶液を東京メディカルテラスに移送し、1バイアルずつ自然解凍し患者に点滴投与します(図6右側:東京メディカルテラスの部分)。
元来自分の免疫細胞ですので副作用はないと考えていますが、万が一何か異常があればその場で対処し、帰宅後も連絡を取り合いながら対応して行きます。
体内に入った樹状細胞は、患者体内のNKT細胞やγσT細胞に対し抗原提示(癌細胞をターゲットとする指令)を行います(図7)。
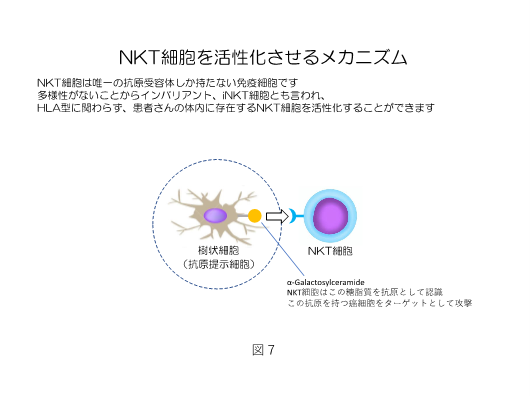
抗癌剤はNKT治療に障害をきたすこともありますが、全てがそうではありません。その説明と癌細胞の免疫逃避に関して追加します。
(3)化学療法によるNKT細胞の活性化
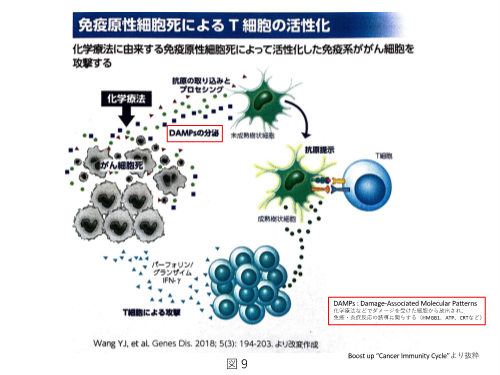
図9に示すように、化学療法(抗癌剤)によって少なからず癌細胞は障害を受け、死滅する癌細胞もいます。死滅した癌細胞からDAMPs(Damage-Asssociated Molecular Patterns)、すなわち癌抗原が逸脱します。この抗原を樹状細胞が取り込みNKT細胞に抗原提示を行うことで癌細胞への攻撃が始まります。従って、抗癌剤自体が癌細胞を破壊するだけではなく、免疫細胞のサイクルも回し始めているのです。ただしここに癌細胞の免疫逃避(免疫学的寛容)が立ちはだかります。
(4)癌細胞の免疫逃避に対する対処方法
癌細胞は常に免疫からの逃避をおこなっています。転移して逃げるだけではなく、自らをベールで覆い免疫細胞から身を隠しています。そのベールを剥がしてくれるのがニボルマブ(オプジーボ®︎)やペムブロリズマブ(キイトルーダ®︎)です。ここでは詳細な機序の説明は割愛しますが、このベールを剥がすことで、NKT細胞は簡単に癌細胞を見つけ攻撃することができるようになります。しかし癌細胞は新たなベールを見つけて再度身を隠してしまう可能性がありますので、できる限り早急に免疫細胞の攻撃が完成しなければならないと判断されます。
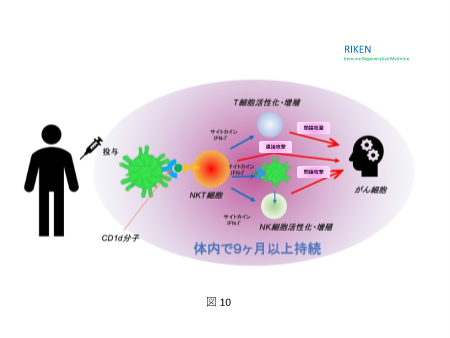
もう一つ重要なことは、このNKT細胞による癌免疫治療効果は抗癌剤の効果と異なり、長期に効力を発揮するということです。図10に示すように1年近く持続効果が認められています。
(5)治療効果判定とその時期(院内スケジュール・プロトコル)
癌治療を行う場合、その方法によっても効果判定時期と方法が異なりますが、NKT細胞による癌免疫治療は、手術と同様の考え方で評価して行くべきであると思っております。個々人の癌腫と病態によっても異なると判断されますが、成熟樹状細胞投与スケジュールに合わせた血液検査(腫瘍マーカー等)や画像診断を行います。その後1ヶ月から4ヶ月の期間に予定を組みますが、腫瘍縮小効果があり、かつ臨床症状も落ち着いていれば(PR以上)、年1回の精査で良いと考えます。その上で下記評価を行い、本人・家人に説明を行います。他院への情報提供の必要があれば同時に情報提供書を作成します。
| 総合評価 | 説明 |
|---|---|
| CR (Complete Response) | 標的病変の完全消失、かつnew lesion出現なし |
| PR (Partial Response) | 標的病変の径和が30%縮小 |
| PD (Progressive Disease) | 標的病変の径和が20%以上増大 |
| SD (Stable Disease) | 標的病変の変化が少ない |
画像検査は、レントゲン検査、内視鏡検査、超音波検査、CT、MRI、PET-CT等で行います。腫瘍の評価可能病変を設定した上で、腫瘍マーカーや臨床症状を含む身体所見と照合し、診察を行って総合評価を致します。
当院では、血液検査、胸・腹部レントゲン検査、胃カメラ、超音波検査を行い、他は連携施設で行います。
(6)予期される効果と副作用
1)効果について
NKT細胞標的治療は、すでに大学等の研究機関で臨床試験が行われ、進行性肺がんや頭頸部癌に十分な効果を示唆する結果が発表されています。しかし治療によって得られる効果は、患者さんの病態、血液状態などによって個人差があります。
当クリニックでは、患者さんが現在治療中(通院中)の病院に協力をお願いし、効果判定に必要な検査データを収集し、検証したいと考えていまが、協力を得られない場合は当院で追加検査をする場合もありますのでご承知おきください。
引き続き不安のない医療を提供できるように、患者さんごとに最適な治療を検討し、場合によって、他施設と連携する治療を行う場合もございます。NKT細胞標的治療は、理論的には全てのがん患者に行うことが可能な治療法ですが、全てのがん患者に対して投与の結果が検証された治療法ではありません。
参考として、医師主導型治験として行われた、肺がんと頭頸部癌に対するNKT細胞標的治療の結果については(7)の①に文献を提示いたします。
2)治療の副作用について
『GMP基準準拠アルファ・ガラクトシルセラミド』を認識させた樹状細胞を投与した後にGrade2以下の副作用として、発熱や全身倦怠感、呼吸困難感などが起こることがあるとされていますが、多くの場合が微熱で2日以内に軽快する軽微なものです。また、ごく稀に軽度のアレルギー症状があるとされますが、心配はありません。
これまでの臨床試験の実績においては、有害事象として、ALT、AST、ALP、CRE、LDHの上昇等が臨床検査値異常として認められましたが、治療を要するレベルには至っていません。しかし、患者さんと連携を取りながら経過観察を行います。
3)アフェレーシスに伴う副作用について
ソケイ部の静脈にカテーテルを挿入し血液を体外循環させますが、カテーテルの穿刺は習熟した医師が局所麻酔を使用して行います。抜去後には十分止血を行いますが、まれに穿刺した箇所に皮下出血を認めることがあります。アフェレーシスは穿刺の緊張から迷走神経反射(めまい、吐き気・嘔吐、徐脈など)を生じないよう留意し、できるだけリラックスをして頂いて行います。心電図モニターを装着し、注意深く観察しながら採取速度を調節し、何らかの症状が出現した際は、アフェレーシスを中断し、適切な対応をすることで、直ちに症状を改善させます。
また、アフェレーシスは体外循環を行いますので、血液が凝固しないよう抗凝固剤を使用します。これに含まれるクエン酸によって血中のカルシウム濃度が低下しますので、予防的カルシウム投与を行いますが、まれに口唇、手指でのしびれなどの低カルシウム血症を来します。カルシウム投与も行いますが、初期症状が認められた時点で体外循環速度を遅くし、急激な血中クエン酸濃度の上昇を抑制した上で、カルシウムを追加投与し症状を改善させます。
また、一過性の血小板減少がみられることもありますが、すぐに回復するため血小板輸血が必要になることはありません。
(7)癌免疫治療に対する文献の紹介
①新しい概念に基づく癌免疫治療―NKT細胞標的治療
NKT cell-targeted anti-cancer immunotherapy based on a novel concept
独立行政法人理研化学研究所統合生命医科学研究センター 谷口 克
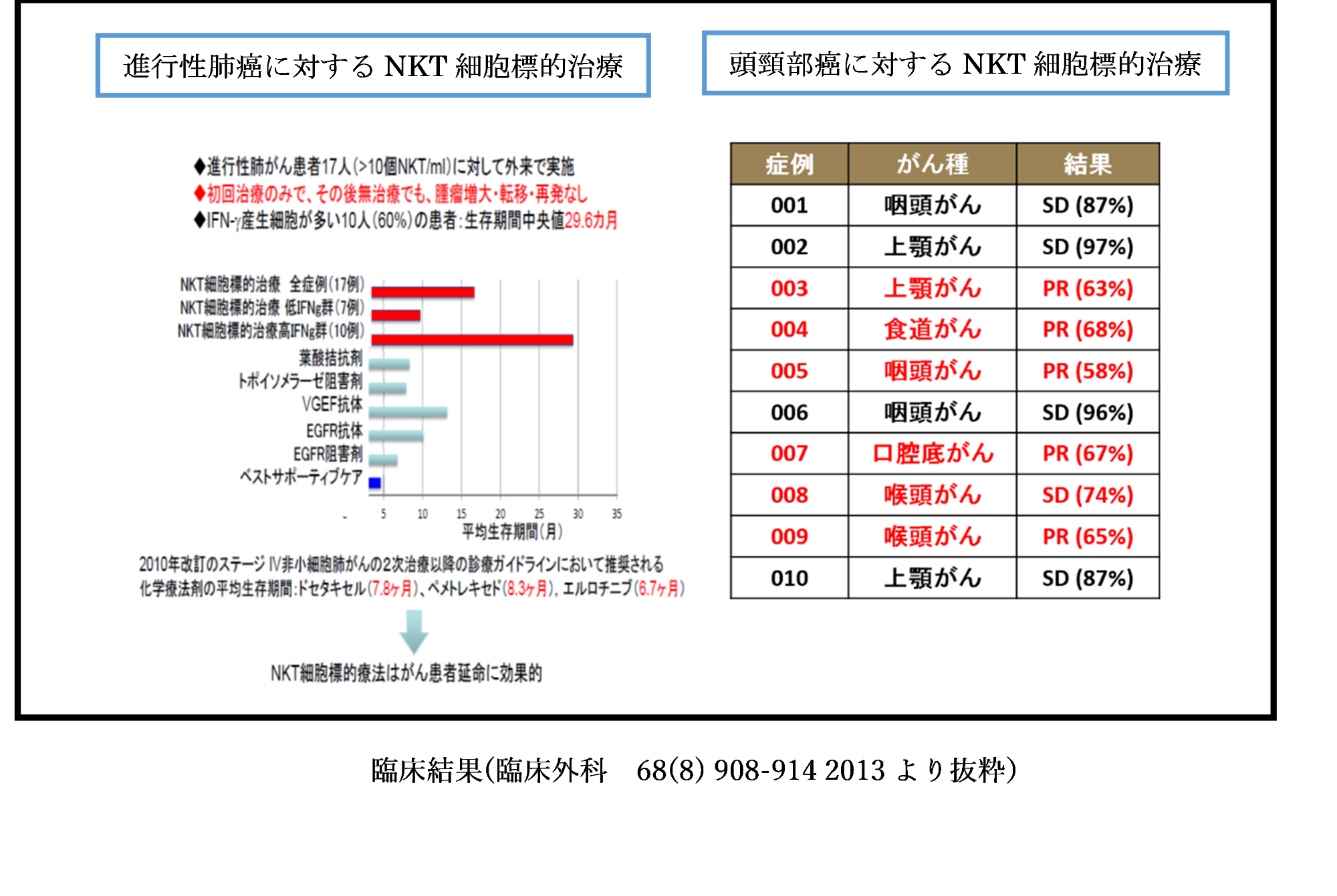
これまでの癌免疫治療は、癌免疫に関わる免疫細胞1種類だけを標的にした治療法であったため、再発が起こることが問題であった。ダオ3世代の癌免疫治療―NKT細胞標的治療として、NKT細胞は患者体内のNK細胞およびキラーT細胞の両方を“増殖・活性化”でき、「HLA発現を失った癌細胞」と「HLA発現のある癌細胞」の2種の癌細胞を同時に排除できる仕組みを利用している。NKT細胞標的治療第Ⅰ/Ⅱa臨床試験では、進行肺癌治療群17例の60%の平均生存率は30ヶ月で、優位な延長が見られた。
臨床外科学会誌 68(8):908–914, 2013
②A Phase I Study of A-Galactosylceramide (KRN7000)–Pulsed Dendritic Cells in Patients with Advanced and Recurrent Non–Small Cell Lung Cancer
Aki Ishikawa,1,2 Shinichiro Motohashi,1,2 Eiichi Ishikawa,1 Hiroki Fuchida,1Kazuko Higashino,1 Mizuto Otsuji,2 Toshihiko Iizasa,2 Toshinori Nakayama,1 Masaru Taniguchi,3 and Takehiko Fujisawa2
1Department of Immunology and 2Thoracic Surgery, Graduate School of Medicine, Chiba University, Chiba, Japan and 3Laboratory for Immune Regulation, RIKEN Research Center for Allergy and Immunology, Yokohama, Kanagawa, Japan
ABSTRACT
Purpose: Human VA24 natural killer T (NKT) cells
bearing an invariant VA24JAQ antigen receptor, the counterpart of murine VA14 NKT cells, are activated by a specific ligand, A-galactosylceramide (AGalCer, KRN7000), in a CD1d-dependent manner. I.v. administration of AGalCer-pulsed dendritic cells (DC) induces significant activation and expansion of VA14 NKT cells in the lung and resulting potent antitumor activities in mouse tumor metastatic models. We did a phase I dose escalation study with AGalCer-pulsed DCs in lung cancer patients.
Experimental Design: Patients with advanced non – small cell lung cancer or recurrent lung cancer received i.v. injections of AGalCer-pulsed DCs (level 1: 5 107/m2; level 2: 2.5 108/m2; and level 3: 1 109/m2) to test the safety, feasibility, and clinical response. Immunomonitoring was also done in all completed cases.
Results: Eleven patients were enrolled in this study. No severe adverse events were observed during this study in any patient. After the first and second injection of AGalCer- pulsed DCs, dramatic increase in peripheral blood VA24
Received 7/22/04; revised 12/3/04; accepted 12/9/04.
Grant support: Program for Promotion of Fundamental Studies in Health Sciences of the Organization for Pharmaceutical Safety and Research (Japan); Ministry of Education, Culture, Sports, Science and Technology (Japan; Grants-in-Aid for Scientific Research, Priority Areas Research no. 13218016; Scientific Research A-2 no. 15209045, Scientific Research B no. 14370107, Advanced and Innovational Research Program in Life Science, and Special Coordination Funds); Ministry of Health, Labor and Welfare (Japan; Grants-in-Aid for Research on Advanced Medical Technology); Kirin Brewery Co.; and Uehara Memorial Foundation.
The costs of publication of this article were defrayed in part by the payment of page charges. This article must therefore be hereby marked advertisement in accordance with 18 U.S.C. Section 1734 solely to indicate this fact.
Note: A. Ishikawa and S. Motohashi contributed equally to this work. Requests for reprints: Toshinori Nakayama, Department of Immunol- ogy, Graduate School of Medicine, Chiba University, 1-8-1 Inohana, Chuo-ku, Chiba 260-8670, Japan. Phone: 81-43-226-2186; Fax: 81-43- 227-1498; E-mail: tnakayama@faculty.chiba-u.jp.
D2005 American Association for Cancer Research.
NKT cells was observed in one case and significant responses were seen in two cases receiving the level 3 dose. No patient was found to meet the criteria for partial or complete responses, whereas two cases in the level 3 group remained unchanged for more than a year with good quality of life.
Conclusions: In this clinical trial, AGalCer-pulsed DC administration was well tolerated and could be safely done even in patients with advanced disease.
(8)治療に関わる費用
初診料:33,000円(税込)
感染症等検査費(初診時のみ):33,000円(税込)
治療費:3,534,000円(税込)
※培養に関わる費用、検体移送費、使用薬剤費、消耗医療機器等の費用も含む
総額:3,600,000円(税込)
*細胞培養が開始された後は返金できません。
【癌治療の担い手】
以上がNKT細胞による癌免疫治療の大枠です。NKT細胞に指令を与えることで癌細胞を排除する方法は、臨床的に理にかなっていますが、すべての癌に有効であるわけではありません。高度進行癌に対して無力であったケースもありますし、逆にNKT癌免疫治療単独で、進行した肺癌や膵癌、子宮癌が劇的に収束したケースもあります。だからこそ私たちは希望を持って診療しています。
私たちは、癌免疫治療を担当いたしますが、患者さんを治すことが目的ですので、むやみにNKT癌免疫治療を行ってはいません。最良の治療法の選択を念頭に置き、まず患者さんの現病歴と治療経過を十分に理解します。すなわち発症時からの検査データや画像データの解析を行うことから始まり、現在までの病態の把握を細かく行います。それまでの治療を無駄にせず将来に生かすためにも最も効果が予想される治療計画を立てなければならないからこそ、専門的評価が必要になります。例えば、どのような手術や放射線治療を受けたのかは専門的判断が必要ですし、現在あるいは将来手術可能なのか不可能なのかの判断もしなければなりません。各種ステント類の留置やポート設置を受けた方など、それぞれに対応しながら診療する必要があります。使用したあるいは使用中の抗癌剤の種類を聞き、副反応や副作用について問診し、アドバイスをいたします。そして治療方針を組み立て、患者さんの希望や意向も加えて判断し、その上で患者さんと向き合い説明をし、患者さんが納得できる治療を進めて行きます。そのため、手術や抗癌剤を熟知した経験豊富な医療者でなければ対応できません。
そして、癌免疫治療を集学的治療の一環として臨床の場に持ち込むために、今まで患者さんが受けてきた治療を理解し、それらを無駄にせず、他の医療機関とも連携した体制を構築することが、良質ながん治療であると考えています。
標準治療の定義はないのですが、ほとんどの保険医は保険診療こそが標準治療だと信じており、未だ自由診療であるNKT細胞標的癌免疫治療を敵視している医師も少なくありませんが、私たちは、癌免疫治療の効果を1症例ごとに正しく評価し、患者さん共に歩んで行きたいと考えています。
現時点では進行癌(全身癌)に対しての各マニュアルは、化学療法(抗癌剤治療)となっています。抗癌剤投与で免疫力低下を招きNKT細胞治療に障害をきたすことはあっても、NKT治療が抗癌剤治療の障害になることはありません。しかし多くの癌治療医は、NKT再治療のような自由診療を選択するなら責任は持てないと言って診療拒否を行います。ナンセンスな言動ですが、日本の実情です。しかし患者に責任を持つということがどういうことなのか考えて欲しいのです。自分の私生活を捨ててでも、患者に寄り添う覚悟があるのでしょうか。覚悟のない医師の身勝手な一言で、患者さんが希望する治療を諦め、生に対する希望も失って悲しい思いをするようなことがないように望みます。
【 まとめ 】
以上、NKT細胞による癌免疫治療についての個人的な意見を含めた解説を行いました。
癌治療は、手術・放射線治療・化学療法・緩和医療そしてそれらを組み合わせる集学的治療があり、癌治療専門医も増えています。しかし患者さんを最後まで診ない専門医が増えているため、癌難民が増加しています。癌病巣をコントロールできず、治療に行き詰まることがあっても患者を見捨てることのない医療でなければなりません。なぜなら医療しか患者さんを幸せにする道はないからです。道がなくなっても道を作ってあげなければなりません。
「もう全ての治療が終わり、これ以上の治療はできません、家族と温泉にでも行きなさい」と言って、不適切な緩和医療を訪問診療の医師や看護師に押し付け、その後は一才の治療を断る施設が増えました。実際、緩和医療研修ではそういう指導をしています。
これ以上の治療を望まず、自宅で家人と過ごすことを第1に考える患者さんにとっては優しい言葉ですが、まだ治療を望んでいる患者さんにとっては残酷な言葉です。本人が治療を望んでいる限り、医療という枠の中に居させてあげなければなりません。医療者は患者さんの希望を叶えることを最大の目標にし、常に最善の医療をし続けなければならないと思っています。
NKT細胞癌治療免疫治療は、患者さんの身体に負担の少ない効果的な治療です。
そして今後iPS-NKT細胞作成によって、体内に0.01%しか存在しないNKT細胞を増やすことができれば、αGalCel認識樹状細胞によるこの治療法が、飛躍的に効果を上げることができると考え、期待しているところです。
東京メディカルテラス
〒107-0061
東京都港区北青山2丁目13-4 青山MYビル4F
TEL:03-6721-1899
FAX:03-6721-0899